-
Partager cette page
La chimie est entre vos mains !
Expérimentarium de chimie
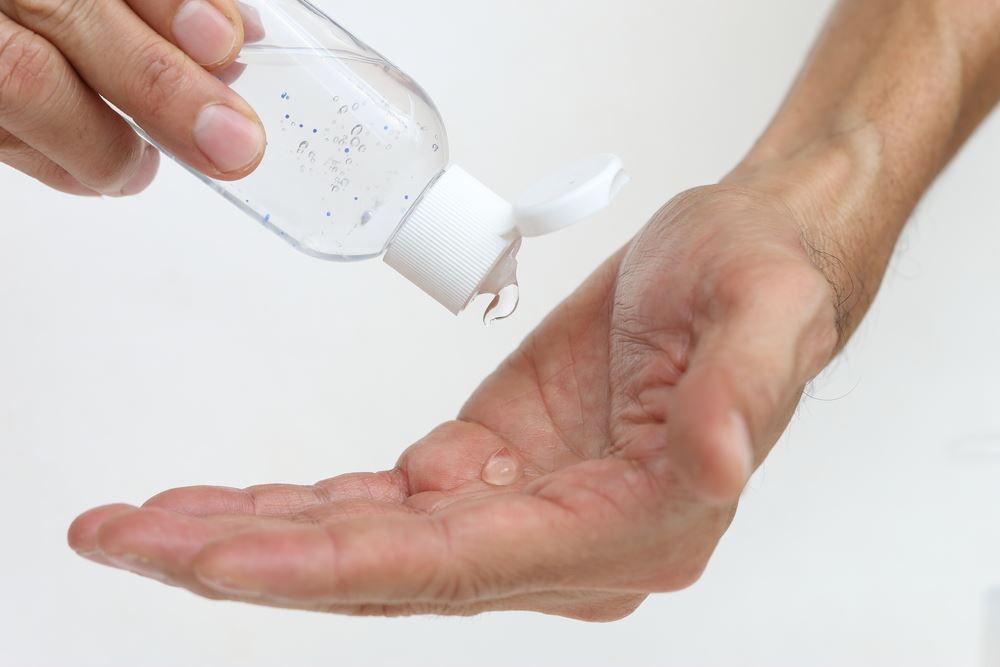
En cette période de crise sanitaire liée au Covid-19, un produit chimique fait beaucoup parler de lui : le gel hydroalcoolique.
La première parade contre le coronavirus, c’est l’hygiène des mains. Un bon lavage des mains avec de l'eau et du savon reste encore la façon efficace la plus simple de se protéger contre la propagation des épidémies.
Un virus (mot qui vient du mot latin uirus, qui signifie humeur, venin, poison, mauvaise odeur, infection) est un agent infectieux qui, contrairement à une bactérie, nécessite un hôte, souvent une cellule, dont il utilise le métabolisme pour se répliquer. Les protéines de surface qui couronnent l’enveloppe des particules virales sont celles qui permettent au virus de s’accrocher aux cellules pour les infecter.
De l’avis d’un groupe d’experts de l’OMS (Organisation mondiale de la Santé), les produits hydroalcooliques peuvent également être utilisés pour l’antisepsie des mains par friction hydroalcoolique. Ces produits permettent en effet l’inactivation rapide et efficace d’un large éventail de micro-organismes qui peuvent être présents sur les mains.
Les produits antiseptiques et désinfectants agissent toutefois de façon momentanée ; ils ne protègent pas contre une nouvelle contamination.
Contrairement aux antiseptiques qui sont appliqués sur des tissus vivants (peau, plaie…), les désinfectants sont utilisés sur des matériaux inertes (meubles, sol, matériel médical…).
Fabriquer son propre gel ?
Quatre produits sont nécessaires à la fabrication d'une solution hydroalcoolique, à savoir de l’alcool, de l'eau oxygénée (ou peroxyde d'hydrogène), du glycérol (ou glycérine) et de l’eau.
L'alcool tue les virus et les bactéries. Plus la concentration en alcool est élevée, plus la solution hydroalcoolique sera efficace. Deux alcools sont principalement utilisés : l’éthanol et l’isopropanol. Leur mécanisme d’action (dénaturation des protéines) nécessite toutefois la présence d’eau, la concentration optimale en alcool se situant à 70 %. Les solutions à base d’alcool sont auto-séchantes et sans effet sur la plupart des matériaux. Toutefois, sur certains acrylates (en particulier le Plexiglas), elles entraînent une opacification de la surface.
Éthanol 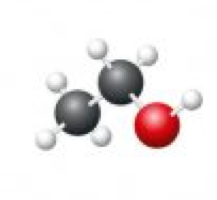
Le peroxyde d’hydrogène n'a aucune action antiseptique sur la peau, mais il élimine les spores bactériennes qui pourraient être potentiellement présentes dans les flacons. C’est la raison pour laquelle il faut attendre au minimum 72 heures avant d'utiliser le gel hydroalcoolique afin que le peroxyde d'hydrogène agisse. Le peroxyde d’hydrogène doit être considéré avec précaution car il peut être particulièrement dangereux. En effet, cet oxydant puissant peut provoquer des réactions violentes (ex. : combustion spontanée, détonation) lorsqu’il entre en contact avec d'autres produits comme des huiles ou de l’alcool. Il peut également provoquer des brûlures à haute concentration.
Peroxyde d'hydrogène 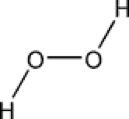
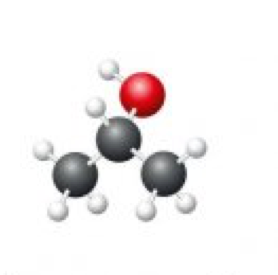
Le glycérol est utilisé dans de nombreuses compositions pharmaceutiques et agit comme humectant. Le glycérol peut être remplacé par d’autres produits émollients pour autant qu’ils puissent se mélanger à l’eau et à l’alcool, mais qu’ils soient aussi non toxiques et non allergéniques.
Glycérol 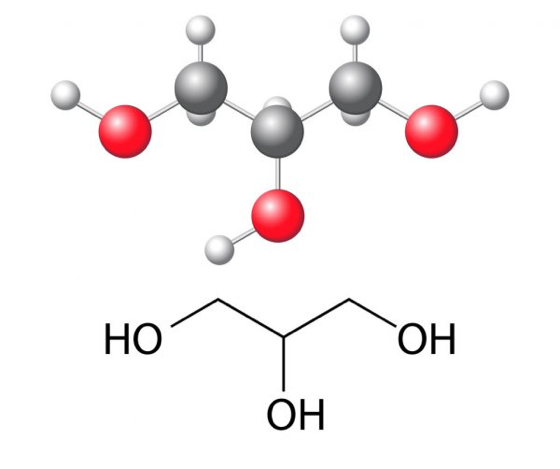
L’eau doit être distillée ou peut être remplacée par de l’eau bouillie, puis refroidie.
Une recherche rapide sur internet montre de très nombreuses sources permettant la fabrication du gel. Toutefois, afin d’éviter toute mauvaise surprise et de mettre en danger sa santé, il est conseillé de suivre certaines précautions d’usage. C’est pourquoi il est fortement conseillé de suivre le document « Guide de production locale » de l’Organisation Mondiale de la Santé qui est à ce jour la meilleure référence [1]. Même si cette « recette » est au départ destinée aux professionnels de la santé, elle est également assez simple à appliquer chez soi.
Une sensation de froid ?
Certains produits peuvent présenter une sensation de froid quand ils sont laissés sur la peau à l’air libre. C’est le cas du gel hydroalcoolique qui, par ailleurs, présente également un séchage particulièrement rapide.
Ces deux phénomènes sont en réalité liés. Quand le gel hydroalcoolique sèche, il s’évapore. Il passe donc de l’état liquide à l’état gazeux. Cela provoque une sensation de froid car l’évaporation, qui est un phénomène endothermique, absorbe la chaleur environnante pour avoir lieu. Résultat : vos mains cèdent de la chaleur et se refroidissent lorsque le gel sèche.
L’eau rafraîchit également, mais moins que l’alcool.
Ce principe impliquant un changement d’état, qui capte ou libère de la chaleur selon le type de processus impliqué, est utilisé dans beaucoup d’appareils aujourd’hui : refroidisseur de PC, réfrigérateur, climatiseur, pompe à chaleur, …
[1] « Guide de Production locale : Formulations des Produits hydroalcooliques recommandés par l’OMS »
Claudine Buess-Herman, Jean-Christophe Leloup, Cécile Moucheron & Nathalie Vaeck
Responsables de l'Expérimentarium de chimie